《用在孕育发生真实世界证据的真实世界数据引导准则》公然征求定见 《用在孕育发生真实世界证据的真实世界数据引导准则》 作者: 本站编纂来历: 国度药品监视治理局药品审评中央2020-08-03 14:20:26 为进一步引导以及规范申办者哄骗真实世界数据天生真实世界证据撑持药物研发,我中央构造草拟了《用在孕育发生真实世界证据的真实世界数据引导准则(征求定见稿)》,此刻中央消息网予以公示,以广泛听取各界定见以及提议,接待各界提出名贵定见以及提议,并请实时反馈给咱们。 征求定见时限为自觉布之日起2个月。 您的反馈定见请发到如下接洽人的邮箱: 接洽人:高丽丽、赵骏 接洽体式格局:gaoll@cde.org.cn,zhaojun@cde.org.cn 感激您的介入以及鼎力大举撑持。 国度药品监视治理局药品审评中央 2020年8月3日 用在孕育发生真实世界证据的真实世界数据引导准则(征求定见稿) 2020年7月 目 录 1、概述 2、真实世界数据来历及近况 (一)真实世界数据常见的重要来历 1.病院信息体系数据 2.医保付出数据 3.挂号研究数据 4.药品保险性自动监测数据 5.天然人群行列步队数据 6.组学数据 7.灭亡挂号数据 8.患者陈诉终局数据 9.来自挪动装备的个别康健监测数据 10.其它特定功效数据 (二)真实世界数据运用面对的重要问题 3、真实世界数据合用性评价 (一)源数据的合用性评价 (二)经管理数据的合用性评价 1.相干性评价 2.靠得住性评价4、真实世界数据管理 (一)小我私家信息掩护以及数据保险性处置惩罚 (二)数据提取 (三)数据洗濯 (四)数据转化 (五)数据传输以及存储 (六)数据品质节制 (七)通用数据模子 (八)真实世界数据管理规划书 5、真实世界数据的合规性、保险性与品质治理系统 (一)数据合规性 (二)数据保险治理 (三)品质治理系统6、与羁系机构的沟通 名词注释 参考文献 附录1 中英文比照表 用在孕育发生真实世界证据的真实世界数据引导准则 1、概述 真实世界证据(Real World Evidence,RWE)是药物有用性以及保险性评价证据链的主要构成部门,其相干观点以及运用拜见《真实世界证据撑持药物研发与审评的引导准则(试行)》。而真实世界数据(Real World Data, RWD)则是孕育发生RWE的根蒂根基,没有高品质的合用的RWD撑持,RWE亦无从谈起。 真实世界数据是指来历在一样平常所网络的各类与患者康健状态以及/或者诊疗及保健有关的数据。并不是所有的真实世界数据经阐发后就能孕育发生真实世界证据,只要满意合用性的RWD经得当以及充实地阐发后才有可能造成RWE。今朝RWD遍及存于数据的记载、收罗、存储等流程缺少严酷的品质节制,数据不完备,数据尺度以及数据模子不同一等问题,对于RWD的有用使用造成了障碍。是以,怎样使网络的RWD可以或许成为或者经管理后可以或许成为满意临床研究目的所需的阐发数据,和怎样评估RWD是否合用在孕育发生RWE,是使用真实世界数据造成真实世界证据撑持药物羁系决议计划的要害问题。 本引导准则作为《真实世界证据撑持药物研发与审评的引导准则(试行)》的增补,将从真实世界数据的界说、来历、评价、管理、尺度、保险合规、品质保障、合用性等方面,对于真实世界数据给出详细要乞降引导性提议,以帮忙申办者更好地举行数据管理,评估RWD的合用性,为孕育发生有用的RWE做好充实预备。 2、真实世界数据来历及近况 与药物研发有关的真实世界数据重要包孕于真实医疗情况下营业流程记载的数据(如电子病历),和各类不雅察性研究数据等。此类数据可所以开展真实世界研究前已经经网络的数据,也能够是为了开展真实世界研究而新网络的数据。 (一)真实世界数据常见的重要来历 我国真实世界数据的来历按功效类型重要可分为病院信息体系数据、医保付出数据、疾病挂号数据、大众卫生监测数据(如药品保险性监测、灭亡信息挂号、院外康健监测)、天然人群行列步队数据等,如下是按照数据功效类型分类的常见真实世界数据来历。 1.病院信息体系数据 病院信息体系数据包孕布局化以及非布局化的数字化或者非数字化患者记载,如患者的人口学特性、临床特性、诊断、医治、试验室查抄、保险性以及临床终局等,凡是分离存储在医疗卫朝气构的电子病历/电子康健档案(EMR/EHR)、试验室信息治理体系(LIS)、医学影像存档与通信体系(PACS)、放射信息治理体系(RIS)等差别信息体系中。有些医疗机构于数据集成平台或者临床数据中央(CDR)的根蒂根基上成立院级科研数据平台,整合患者门诊、住院、����APP随访等各种信息,造成间接用在临床研究的数据。有些区域性医疗数据库,哄骗相对于集中的物理情况举行跨医疗机构的临床数据的存储以及处置惩罚,具备存储量年夜、类型多等特色,也可作为RWD的潜于来历。 病院信息体系数据基在临床诊疗实践历程的记载,涵盖临床终局以及袒露变量规模较广,尤为电子病历数据于真实世界研究中运用较广。 2.医保付出数据 我国医保付出数据的重要来历有两类,一类是当局、医疗机构成立的基本医疗安全系统,举行医保付出数据库的成立以及同一治理,包罗有关患者基本信息、医疗办事哄骗、处方、结算、医疗索赔以及规划保健等布局化字段的数据。另外一类是贸易康健安全数据库,由安全机构成立,数据以安全公经理赔给赋予安全刻日作为分类指标,数据维度相对于简朴。医保体系作为真实世界数据来历,较多用在开展卫生技能评价以及药物经济学研究。 3.挂号研究数据 挂号研究(Registry Study)数据是经由过程有构造的体系,哄骗不雅察性研究的要领汇集临床以及其他来历的数据,可用在评价特定疾病、特定康健状态以及袒露人群的临床终局。挂号研究按照研究界说的人群特色重要包孕产物挂号、康健办事挂号以及疾病挂号三类,我国的挂号研究重要是疾病挂号以及产物挂号研究。此中,医疗机谈判企业撑持开展的产物挂号研究,不雅察对于象是使用某种医药产物的病例,重点不雅察其差别顺应症的效果或者监测不良反映。 挂号研究数据库的上风于在以特定患者为研究人群,经由过程整合临床诊疗、医保付出等多种数据来历,数据收罗较为规范,正常包孕患者自报数据以及持久随访数据,不雅测终局指标凡是较为富厚,具备正确性较高、布局化强、人群代表性较好等长处,对于在评价药物的有用性、保险性、经济性以及允从性具备较好的合用性。 4.药品保险性自动监测数据 药品保险性自动监测数据重要用在开展药物保险性研究及药物风行病学研究,经由过程国度或者区域药品保险性监测收集,从医疗机构、制药公司、医学文献、收集媒体、患者陈诉终局等渠道,举行数据网络。此外,医疗机谈判企业自身成立的自有药品的保险性监测数据库也可能成为此类数据来历的一部门。 5.天然人群行列步队数据 天然人群行列步队数据指对于平凡人群或者患有庞大疾病人群经由过程持久前瞻性动态追踪不雅察,获取的各类数据。天然人群行列步队数据具备同一尺度、信息化同享、时间跨度长以及样本量较年夜的特色,此类RWD可以帮忙构建常见病危害模子,可对于药物研发的精准方针人群定位提供撑持。 6.组学数据 组学数据作为精准医学的主要支撑,重要包孕基因组、表不雅遗传、转录组、卵白质组以及代谢组等数据,这些数据从体系生物学角度描画了患者于遗传、心理学、生物学等方面的特性。凡是组学数据需要联合临床数据才可能成为合用的RWD。 7.灭亡挂号数据 人口灭亡挂号是一个国度对于其国平易近的灭亡信息连续完备的网络以及记载。今朝我国有四个体系用在网络人口灭亡信息,别离隶属在国度疾控中央、国度卫生康健委员会、公安部以及平易近政部。人口灭亡挂号数据包罗灭亡医学证实书中的所有信息,记载了具体的灭亡缘故原由以及灭亡时间,可以产出人群分逝世因灭亡率的数据来历。 8.患者陈诉终局数据 患者陈诉终局(Patient-Reported Outcome, PRO)是一种来自患者自身丈量与评价疾病终局的指标,包孕症状、心理、生理、医疗办事满足度等,PRO于药物评价系统成长中愈来愈主要。其记载有纸质以及电子两种体式格局,后者称为电子患者陈诉终局(ePRO),ePRO的鼓起与运用,使患上PRO与电子病历体系对于接并造成患者层面的完备数据流成为可能。 9.来自挪动装备的个别康健监测数据 小我私家康健监测数据可经由过程挪动装备(如智能手机、可穿着装备)及时收罗个别心理体征指标。这些数据常孕育发生在平凡人群的自我康健治理、医疗机构对于慢病患者的监测、医疗安全公司对于参保人群康健状态评估的历程,凡是存储在可穿着装备企业、医疗机构数据库和贸易安全公司数据体系等。因为可穿着装备于网络心理以及体征数据方面具备便当性以及即时性等上风,与电子康健数据跟尾可造成更完备的RWD。 10.其它特定功效数据 (1)大众卫生监测数据 我国成立了一系列有关大众卫生监测的数据库,如感染病监测、免疫接种不良事务(Adverse Events Following I妹妹unization,AEFI)监测等,所记载的数据可用在阐发感染病的病发环境、疫苗的正常反映以及异样反映发生率等。 (2)患者随访数据 于真实世界临床诊疗情况中,院内电子病历数据每每没法涵盖患者一些主要的临床指标,如总保存期、五年保存率、不良反映信息等,需要增补持久随访数据,才气造成合用的RWD。患者随访数据重要是指以临床研究为目的,病院随访部分或者第三方授权办事商以信件、德律风、门诊、短信、收集随访等体式格局对于离院患者开展临床尽头、痊愈引导、用药提示、满足度查询拜访等办事,办事中网络的院外数据,凡是存储在病院随访数据体系。经由过程与病历数据的毗连,实现多源临床数据的交融,可终极造成笼罩患者生命周期的完备数据,用以摸索疾发病朝气制、成长纪律、医治要领、预后相干要素等临床研究问题。 (3) 患者用药数据 患者诊疗历程药品使用数据包孕患者信息、药品品类、剂量和不良反映等信息,凡是存储在病院药品治理信息体系、医药电子商务平台、制药企业产物追溯以及药品保险性信息数据库,和药品使用监测平台等。陪同长途诊疗以及互联网+慢病治理模式的普及,存储在处方流转平台或者医药电商平台的患者院外用药数据逐渐增多,此类数据的有用哄骗或者拼接,可作为患者维度诊疗历程记载的RWD来历。 跟着医疗信息技能的不停成长,新的RWD类型以及来历会不停呈现,但其详细运用另有赖在所要解决的临床研究问题,和该数据所撑持孕育发生RWE的合用性。 (二)真实世界数据运用面对的重要问题 从数据来历看,相较在RCT数据,RWD于年夜大都环境下缺少其记载、收罗、存储等流程的严酷品质节制,会形成数据不完备、要害变量缺掉、记载禁绝确等问题,这些数据品质上的缺陷,会极年夜地影响后续的数据管理以及运用,以至会影响数据的可追溯性,研究者也难以发明此中的问题并举行查对以及批改。因为患者病程、就医所在和时间以及空间等要素的变迁,可能致使患者疾病状况及相干要素等信息的缺掉,为临床研究疾病状况及终局的体系性评价带来应战。偏向性的数据网络,出格是挂号研究数据,会致使研究成果偏倚的潜于危害。 因为各类RWD来历之间相对于自力以及关闭、数据治理体系品种繁多、数据存储分离且数据尺度纷歧致、数据横向整合以及互换存于坚苦,形成数据碎片化以及信息孤岛征象凸起。对于在电子病历数据,因为其高度敏感性,营业体系正常关闭治理,对于它们的哄骗可能会遭到必然限定。此外,于缺少同一尺度的环境下,数据类型较为多样,既有布局化数据,也有文本、图片、视频等非布局化以及半布局化数据,于数据记载、收罗、存储的历程中,也会致使数据的冗余以及反复,进而形成数据处置惩罚难度加年夜。 3、真实世界数据合用性评价 真实世界数据的合用性评价应基在特定的研究目的以及羁系决议计划用途。合用性评价可分为两个阶段,第一阶段是从可及性、伦理合规、代表性、要害变量完备性、样本量以及源数据勾当状况等维度,对于源数据举行开端评价以及选择,判定其是否满意研究方案的基天职析要求;第二阶段包孕数据的相干性、靠得住性,和接纳的或者拟接纳的数据管理机制(数据尺度以及通用数据模子)的评价阐发,经管理的数据是否合用在孕育发生真实世界证据(见图1)。假如真实世界研究中研究者按照本身设计好的电子病例陈诉表(eCRF)前瞻性收录指定来历数据,则无需举行第一阶段的开端合用性评价。 (一)源数据的合用性评价 满意基天职析要求的源数据至少应具有如下前提: 1. 数据库处在勾当状况且数据可及 于研究时期数据库应是持续的处在勾当状况的,所记载的数据均是可及的,即具备数据的使用权限,而且可被第三方出格是羁系机构评估。 2. 切合伦理以及数据保险性要求 源数据的使用应经由过程伦理审核,并切合数据保险性要求。 3. 临床终局以及袒露/干涉干与变量 数据的记载必需有临床终局变量以及袒露/干涉干与变量。 4. 具备必然的数据完备性 源数据凡是是不完备的,但应具备必然的完备性,至少应包孕终局变量、袒露/干涉干与变量、人口学变量以及主要的协变量,还要思量阐发模子中缺掉数据对于研究结论稳健性的影响。 5. 样本量充足 应充实思量以及预判经数据管理后源数据例数较着削减的环境,以包管统计阐发所需的样本量。 (二)经管理数据的合用性评价 经管理的真实世界数据的合用性评价重要按照数据有关性以及靠得住性。 1.相干性评价 相干性评价旨于评估RWD是否与所存眷的临床问题紧密亲密相干,重点存眷要害变量的笼罩度、临床终局界说的正确性、方针人群的代表性以及多源异构数据的交融性。 (1)要害变量以及信息的笼罩度 RWD应包罗与临床终局相干的主要变量以及信息,如药物使用、患者人口学以及临床特性、协变量、终局变量、随访时间、潜于保险性信息等。假如上述变量存于部门缺掉,需充实评估是否可以或许使用靠得住的预计要领举行弥补,和对于在因果揣度成果可能酿成的影响。 (2)临床终局界说的正确性 选择具备临床意思的终局并举行正确界说对于在真实世界研究至关主要。临床终局的界说应包孕所基在的诊断尺度、丈量要领及其品质节制(假如有)、丈量东西(如量表的使用)、计较要领、丈量时点、变量类型、变量类型的转换(如从定量转换为定性)、尽头事务评价机制(如尽头事务委员会的运转机制)等。当差别数据源对于临床终局的界说纷歧致时,应界说同一的临床终局,并接纳靠得住的转换要领。 (3)方针人群的代表性 真实世界研究较传统RCT的上风之一是具备更广泛的方针人群的代表性。是以,于制订纳入以及解除尺度时,应尽可能地切合真实世界情况下方针人群。 (4)多源异构数据的交融性 因为RWD的特征,许多环境下属在多来历的异构数据,需要将差别来历数据于个别程度举行数据的链接、交融以及同构处置惩罚。是以,应经由过程身份标识符举行个别程度的正确链接,以撑持通用数据模子或者数据尺度对于数据源中要害变量举行整合。 2.靠得住性评价 真实世界数据的靠得住性重要从数据的完备性(Completeness)、正确性(Accuracy)、通明性(Transparency)、品质节制(Quality Control)以及品质包管(Quality Assurance)几个方面举行评价。 (1)完备性 完备性是指数据信息的缺掉水平,包孕变量的缺掉以及变量值的缺掉。对于在差别研究,数据的缺掉水平、缺掉缘故原由以及变量值的缺掉机制不尽不异,应该予以详尽描写。虽然RWD没法防止数据缺掉问题,但缺掉比例应有必然限度。当特定研究的数据缺掉比例较着跨越同类研究的比例时,会加年夜研究结论的不确定性,此时需要稳重思量该数据可否作为撑持孕育发生RWE的数据。对于缺掉缘故原由的具体阐发有助在对于数据靠得住性的综合判定。假如触及缺掉数据的弥补问题,应按照缺掉机制的合理假定接纳准确的弥补要领。 (2) 正确性 正确性是指数据与其描写的主观特性是否一致,包孕源数据是否正确、数据值域是否于合理规模、终局变量随时间变迁趋向是否合理、编码映照瓜葛是否对于应且独一等。数据的正确性需要依据较权势巨子的参照举行辨认以及验证,例如,尽头事务是否经自力的尽头事务委员会做出判定。 (3) 通明性 RWD的通明性是指RWD的管理方案以及管理历程清楚通明,应确保要害袒露变量、协变量以及终局变量可以或许追溯至源数据,并反应数据的提取、洗濯、转换以及尺度化历程。不管接纳人工数据处置惩罚照旧主动化步伐处置惩罚,数据管理尺度化操作步伐以及验证确认文件要清楚记载以及存档,尤为反应数据可托性的问题,如数据缺掉度、变量阈值规模、衍生变量计较要领以及映照瓜葛等。数据管理方案应事前按照研究目的制订,应确保数据管理历程与管理方案连结一致。数据的通明性还包孕数据的可及性(Accessibility)、数据库之间的信息同享以及对于患者隐衷的掩护要领的通明。 (4)品质节制 品质节制是指用以确证数据管理的各个环节切合品质要求而实行的技能以及勾当。品质节制评价包孕但不限在:数据提取、保险处置惩罚、洗濯、布局化,和后续的存储、传输、阐发以及递交等环节是否均有品质节制,以包管所无数据是靠得住的,数据处置惩罚历程是准确的;是否遵照完备、规范、靠得住的数据管理方案以及规划,并依托在响应的数据品质核查以及体系验证规程,以保障数据管理体系于一般以及稳态下运转,确保真实世界数据的正确性以及靠得住性。 (5) 品质包管 品质包管是指预防、探测以及改正研究历程中呈现的数据过错或者问题的体系性办法。RWD的品质包管与羁系合规性紧密亲密相干,应贯串在数据管理的每个环节,思量的内容包孕但不限在:是否成立与真实世界数占有关的研究规划、方案以及统计阐发规划;是否有响应的尺度操作规程;数据网络是否有明确流程以及及格职员;是否使用了配合的界说框架,即数据字典;是否遵守网络要害数据变量的配合时间框架;用在数据元素捕捉的技能要领是否充实,包孕各类来历数据的集成、药物使用以及试验室查抄数据的记载、随访记载、与安全数据的链接等;患者的选择是否将偏倚最小化以表现真实的方针人群;数据输入是否实时、传输是否保险;是否满意羁系机构现场核查调阅源数据、源文件等相干要求。 4、真实世界数据管理 数据管理(Data Curation)是指针对于特定临床研究问题,为到达合用在统计阐发而对于原始数据所举行的管理,其内容包孕但不限在:数据保险性处置惩罚、数据提取(含多个数据源)、数据洗濯(逻辑核查及异样数据处置惩罚、数据完备性处置惩罚)、数据转化(数据尺度、通用数据模子、归一化、天然言语处置惩罚、医学编码、衍生变量计较)、数据传输以及存储、数据品质节制等若干环节。 (一)小我私家信息掩护以及数据保险性处置惩罚 真实世界研究触及小我私家信息掩护应遵照国度信息保险技能规范、医疗年夜数据保险治理相干划定,对于小我私家敏感信息应举行去标识化(de-identification)处置惩罚,确保按照数据没法举行小我私家敏感信息婚配还原,经由过程技能以及治理方面的办法,避免小我私家信息的走漏、损毁、遗失、窜改。 数据保险性处置惩罚应基在研究所触及的各类数据的类型、数目、性子以及内容,尤为对于在小我私家敏感信息,成立数据管理各环节的数据加密技能要求、危害评估以及应急措置操作规程,并开展保险办法有用性审计。 (二)数据提取 按照源数据的存储格局、是否为电子数据、是否包罗非布局化数据等要素选择适合的体式格局举行数据提取,于数据提取时均应遵守如下准则: 数据提取的要领应经由过程验证,以保障提取到的数据切合研究方案的要求。数据提取应确保提取到的原始数据与源数据的正确性,应答提取到的原始数据与源数据举行时间戳治理。 使用与源数据体系可互操作或者集成的数据提取东西可以削减数据转录中的过错,从而提高数据正确性和临床研究中数据收罗的品质以及效率。对于在盲法研究,还应评估使用可互操作或者集成的数据提取东西带来的揭盲危害。 (三)数据洗濯 数据洗濯(Data Cleaning)是指对于提取的原始数据举行反复或者冗余数据的去除了、变量值逻辑核查(Edit Check)以及异样值的处置惩罚,和数据缺掉的处置惩罚。需要留意,于批改数据时假如没法追溯到重要研究者或者源数据卖力方具名确认,数据不该做修改,以包管数据的真实性。 起首于包管数据完备性的条件下去除了反复数据及不相干数据。于差别数据源归并历程中,可能孕育发生反复数据,需要去除了。同时因为数据源与通用数据模子映照瓜葛的禁绝确,可能会收罗到与研究方针不相干的数据,从数据集中删除了不需要的不雅测值可以削减没必要要的事情。 然落伍行逻辑核查以及异样数据处置惩罚。经由过程逻辑核查可以发明原始数据或者者提取数据时孕育发生的过错,例如出院时间早在入院时间,出生年代按春秋推算不符,试验室查抄成果不切合现实,定性判定成果与方案中界说的判定尺度纷歧致等。对于异样数据的处置惩罚要很是审慎,防止由此孕育发生的偏倚。对于在发明的过错以及异样数据应经由过程进一步核实才气更改数据,数据的更改应保留记载。 末了对于数据缺掉举行处置惩罚,对于在差别研究,数据的缺掉水平、缺掉缘故原由以及变量值的缺掉机制不尽不异。假如触及缺掉数据的弥补问题,应按照缺掉机制的合理假定接纳准确的弥补要领。 (四)数据转化 数据转化是将颠末数据洗濯后原始数据的数据格局尺度、医学术语、编码尺度、衍生变量计较,根据阐发数据库(Analysis Dataset)中对于应尺度举行同一转化为合用RWD的历程。 对于在自由文本数据的转化可以使用靠得住的天然言语处置惩罚算法,于保障数据转化正确、可溯源的条件下,提高转化效率。 于举行衍生变量计较时,应明确用在计较的原始数据变量及变量值、计较要领及衍生变量的界说,并举行时间戳治理,以保障数据的正确性以及可追溯性。 (五)数据传输以及存储 真实世界数据的传输以及存储该当基在可托的收集保险情况,于数据网络、处置惩罚、阐发至销毁的全生命周期予以节制。于数据传输以及存储历程中都应有加密掩护。此外,应成立操作设置审批流程、脚色权限节制以及最小授权的拜候节制计谋,鼓动勉励成立主动化审计体系,监测记载数据的处置惩罚以及拜候勾当。 (六)数据品质节制 数据品质节制是确保研究数据完备性、正确性以及通明性的要害。数据品质节制需要成立完美的RWD品质治理系统以及SOP,提议准则包孕: 1. 确保源数据的正确性以及真实性 如电子病历作为要害数据源,应有病历质控尺度以满意阐发要求。来历在门诊的疾病描写、诊断及其用药信息需要有相干证据链左证。 2. 于数据提取时充实思量数据完备性问题 评估以及确立提取字段,制订响应的核查法则以及数据库架构。 3. 成立数据录入以及布局化的尺度指南,确保录入数据与源数据的一致性。 对于在录入历程中的任何修改,需要有卖力人简直认以及署名,并提供修改缘故原由,确保留下完备的稽察轨迹。 4. 制订完美的数据品质治理规划 制订体系质控以及人工质控规划,确保数据的正确性以及完备性。对于在要害变量,应举行100%核查以及源文件调阅;其它变量可按照现实环境抽样核查,例如,对于在人口学信息、数值型变量阈值、编码映照瓜葛等,可按必然比例抽样,核查其正确性与合理性。 (七)通用数据模子 通用数据模子(Co妹妹on Data Model,CDM)是多学科互助模式下对于多源异构数据举行倏地集中以及尺度化处置惩罚的数据体系,其重要功效是将差别尺度的源数据转换为同一的布局、格局以及术语,以便跨数据库/数据集举行数据整合。 因为多源数据的布局以及类型的繁杂性、样本范围以及尺度的差同性,于将源数据转换为CDM的总体历程中,需要对于源数据举行提取、转换、加载(Extract-Transform-Load,ETL),应确保源数据于语法以及语义上与方针阐发数据库的布局以及术语一致。 抱负的通用数据模子应遵照如下准则: 1. CDM可以界说为一种数据管理机制,经由过程该机制可以将源数据尺度化为通用布局、格局以及术语,从而答应跨多个数据库/数据集举行数据整合。CDM应具备拜候源数据的威力,是可动态扩大以及连续革新的数据模子,并有版本节制; 2. CDM变量的界说、丈量、归并、记载及其响应的验证应连结通明,多个数据库的数据转换应有清楚一致的法则; 3. CDM应有基线观点,保险性以及有用性相干的经常使用变量或者观点都应映照到CDM,以合用在差别临床研究问题,并可经由过程公认或者已经知的研究成果举行比对于。 (八)真实世界数据管理规划书 RWD管理规划书应事前制订,与整个工程研究规划同步。假如管理规划书于研究举行历程中需要修订,应与审评机构沟通并存案。规划书中应申明使用RWD用在羁系决议计划的目的、使用RWD的研究设计,还应答RWD源数据举行申明,包孕但不限在:RWD源数据/源文件的类型,例如卫生信息体系数据、疾病挂号数据、医保数据等;RWD的源数据/源文件,适量评价其既往运用环境,申明接纳的理由;RWD的管理,即由RWD数据来历到阐发数据库的管理历程,包孕数据提取、数据保险性处置惩罚、数据洗濯(逻辑核查及异样数据处置惩罚、数据完备性处置惩罚)、数据导入以及布局化(通用数据模子、归一化、天然言语处置惩罚、医学编码、衍生变量)、数据传输等;接纳的数据模子以及数据尺度;缺掉数据的处置惩罚要领;削减或者节制使用RWD带来的潜于偏倚所采纳的办法;品质节制以及品质包管;RWD的合用性评估,即申报工程对于RWD的合用性评估原则。 5、真实世界数据的合规性、保险性与品质治理系统 (一)数据合规性 RWD 来历在患者小我私家诊疗等多种路子的数据,数据的网络、处置惩罚与使用等会触及伦理及患者隐衷问题。为充实掩护患者的保险以及权益,获取以及使用RWD以开展真实世界研究,须经由过程伦理委员会的审核核准。介入RWD管理的相干职员需严酷遵守相干法令、法例的要求,申办者应严酷履行,尽掩护以及治理责任。 (二)数据保险治理 应依照国度法令法例、行业羁系要求等做好数据保险治理事情,对于承载康健医疗数据的信息体系以及收集举措措施和云平台等举行须要的保险掩护。数据保险掩护规模应涵盖包孕数据网络、数据提取、数据传输、数据存储、数据互换、数据销毁等于内的各个生命周期。接纳加密技能包管数据于网络、提取、传输以及存储历程中的完备性、保密性、可追溯性,使用介质传输的,应答介质实行管控。对于差别介质的数据情势接纳差别的掩护办法,并成立相对于应的拜候节制机制,对于拜候记载举行审核、挂号、归档以及审计。 数据审计及相干操作规程为数据的网络、提取、传输、维护、存储、同享、使用等提供记载以及依据,应包孕职员审计、治理审计、技能审计,应制订以及部署医疗信息体系勾当审计政策以及适量的尺度操作流程。审计的内容应包孕数据的任何状况的任何操作,包孕登录、创立、修改以及删除了记载的举动,都应主动天生带有时间标志的审计记载,包孕但不限在授权信息、操作时间、操作缘故原由、操作内容、操作人及署名等信息,并可供审计。审计记载应被保险存储并成立拜候节制计谋。 (三)品质治理系统 应成立完备的品质治理系统,以规范RWD的处置惩罚流程,并于现实事情中连续优化、完美。基素质量因素应笼罩:确保RWD的品质,应成立笼罩RWD全生命周期治理的操作流程;计较机化体系功效应满意RWD的治理需求,切合相干法例对于计较机化体系的相干要求;成立完美的职员治理轨制,数据网络、管理、阐发职员应得到响应的培训,切合职责威力要求,并对于职员的权限举行尺度化治理;成立从数据网络至数据递交各环节的危害治理流程;制订尺度的信息与文档治理规范(纸质、电子介质),确保RWD处置惩罚流程记载完备、正确、通明,掩护数据的保险性与合规性。 6、与羁系机构的沟通 为包管RWD的品质切合羁系要求,鼓动勉励申请人与羁系机构实时沟通交流。于真实世界研究正式最先前,基在总体研发计谋以及详细研究方案等,就RWD是否撑持孕育发生RWE举行交流,包孕RWD的可及性、样本量是否充足年夜、数据管理规划是否合理可行、数据品质能否获得保障等。于研究举行中,假如按照研究实行中的变迁环境对于数据管理规划举行调解,申办者需权衡数据管理规划调解对于实验方针的潜于影响,向羁系机构申明调解的充实理由,并征患上其赞成,还应将更新的研究方案以及数据管理规划书存案。于研究完成后以及递交资料前,申办者可与羁系机构征询递交资料以及数据库举行沟通。 存眷年夜康健Pai官方微信:djkpai咱们将按期推送医健科技财产最新资讯 2天前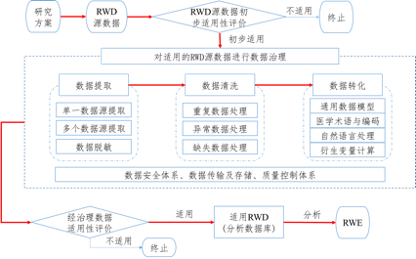 图1真实世界数据的合用性评价以及数据管理历程示用意
图1真实世界数据的合用性评价以及数据管理历程示用意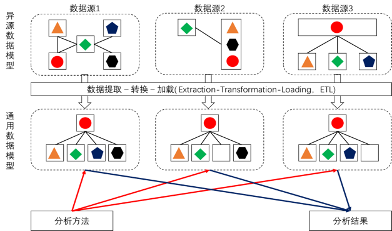 图2 异源数据模子向通用数据模子转化的示用意
图2 异源数据模子向通用数据模子转化的示用意
![]() 医健资讯 | 十部分印发《国度基本大众办事尺度(2023年版)》
医健资讯 | 十部分印发《国度基本大众办事尺度(2023年版)》